Carbon disulfide
Carbon disulfide hay đisulfide carbon là một chất lỏng không màu dễ bay hơi với công thức hóa học CS2. Hợp chất này là một dung môi không phân cực, không màu khi tinh khiết, thường được sử dụng làm nguyên liệu trong tổng hợp hóa hữu cơ ở cả cấp công nghiệp. Nó có mùi giống như "ete", nhưng các mẫu công nghiệp thông thường chứa các tạp chất có mùi khó ngửi, như carbonyl sulfide.[1]
| Carbon disulfide | |
|---|---|
 Carbon disulfide | |
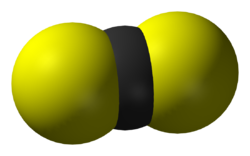 | |
| Danh pháp IUPAC | Methanedithione |
| Tên khác | Carbon disulfide, dithiocacbonic anhydride, carbon bisulfide, bisulfide carbon |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| Số EINECS | |
| Số RTECS | FF6650000 |
| Ảnh Jmol-3D | ảnh |
| SMILES | đầy đủ
|
| Thuộc tính | |
| Công thức phân tử | CS2 |
| Khối lượng mol | 76,139 g/mol |
| Bề ngoài | Lỏng không màu Không tinh khiết: vàng nhạt |
| Khối lượng riêng | 1,261 g/cm³ |
| Điểm nóng chảy | −110,8 °C (162,3 K; −167,4 °F) |
| Điểm sôi | 46,3 °C (319,4 K; 115,3 °F) |
| Độ hòa tan trong nước | 0,29 g/100ml (20°C) |
| Chiết suất (nD) | 1,6295 |
| Cấu trúc | |
| Hình dạng phân tử | Tuyến tính |
| Mômen lưỡng cực | Không |
| Các nguy hiểm | |
| MSDS | ICSC 0022 |
| Phân loại của EU | Dễ bắt cháy (F) Repr. Cat. 3 Độc hại (T) Kích ứng (Xi) |
| Chỉ mục EU | 006-003-00-3 |
| NFPA 704 |
|
| Chỉ dẫn R | R11, R36/38, R48/23, R62, R63 |
| Chỉ dẫn S | S1/2, S16, S33, S36/37, S45 |
| Điểm bắt lửa | -30°C |
| Nhiệt độ tự cháy | 90°C |
| Giới hạn nổ | 1,3–50% |
| LD50 | 3,188 mg/kg |
| Các hợp chất liên quan | |
| Hợp chất liên quan | Carbon dioxide Cacbonyl sulfide |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trong trạng thái tiêu chuẩn của chúng (ở 25 °C [77 °F], 100 kPa). | |
Phổ biến và sản xuất
sửaMột lượng nhỏ carbon disulfide được giải phóng ra từ các vụ phun trào núi lửa và các đầm lầy. CS2 từng được sản xuất bằng cách kết hợp carbon (hay than cốc) và lưu huỳnh ở nhiệt độ cao. Phản ứng có nhiệt độ thấp, chỉ cần 600 °C sử dụng khí thiên nhiên như là nguồn carbon với xúc tác là silica gel hay alumina:[1]
Phản ứng là tương tự như phản ứng đốt cháy methan. Mặc dù nó là đồng electron với carbon dioxide, nhưng CS2 rất dễ bắt cháy:
Phản ứng
sửaSo sánh với CO2, CS2 là hoạt hóa hơn về phía ái lực hạt nhân và rất dễ dàng bị khử. Các khác biệt này trong độ hoạt hóa có thể coi là do khả năng cung cấp π yếu hơn của các trung tâm sulfido, làm cho carbon trở thành ái lực điện tử hơn. Nó được sử dụng rộng rãi trong tổng hợp các hợp chất hữu cơ chứa lưu huỳnh như natri metam, một chất xông đất và được sử dụng rộng rãi trong sản xuất vải viscoza mềm.
Thêm vào các chất ái lực hạt nhân
sửaCác chất ái lực hạt nhân như các amin tạo ra các dithiocacbamat:
- 2R2NH + CS2 → [R2NH2+][R2NCS2−]
Các xanthat tạo thành một cách tương tự từ các alkoxit:
- RONa + CS2 → [Na+][ROCS2−]
Phản ứng này là nền tảng của sản xuất xenluloza tái sinh, thành phần chính của viscoza, rayon và xenlophan. Cả xanthat và thioxanthat tương ứng (sinh ra từ xử lý CS2 với các thiolat natri) đều được sử dụng như là tác nhân tách đãi trong chế biến, xử lý khoáng vật.
Natri sulfide tạo ra thiocarbonat màu đỏ cam:
- Na2S + CS2 → [Na+]2[CS32−]
Clo hóa
sửaClo hóa CS2 là phương thức chính tạo ra carbon tetraclorua:[1]
Phản ứng này thông qua hợp chất trung gian là thiophotgen, CSCl2.
Hóa học điều hợp
sửaCS2 là phối thể cho nhiều phức chất kim loại, tạo thành các phức chất pi. Một ví dụ là CpCo(η2-CS2)(PMe3)[2].
Có sẵn thương mại
sửaCS2, là chất dễ bắt cháy và có nhiệt độ tự kích cháy thấp, không thể dễ dàng vận chuyển bằng các phương tiện vận tải thông thường. Xuất khẩu toàn thế giới của hóa chất này là không đáng kể.
Mẫu cơ sở nitơ lỏng nén
sửaCông ty Alfa Aesar là công ty đầu tiên giới thiệu carbon disulfide trong dạng chai nén chứa dung dịch nitơ lỏng nén, tác nhân kết đôi, chất ổn định và carbon disulfide, với hàm lượng carbon disulfide hoạt hóa là 85%. Hòa loãng với nitơ làm cho dung dịch trở thành không bắt cháy. Tuy nhiên, năm 2007 Alfa Aesar đã ngừng bán các mẫu carbon disulfide.
Tác động tới sức khỏe
sửaỞ nồng độ cao, carbon disulfide có thể đe dọa tới tính mạng do nó ảnh hưởng tới hệ thần kinh. Dữ liệu an toàn có ý nghĩa đến từ công nghiệp sản xuất rayon viscoza, nơi mà cả carbon disulfide lẫn một lượng nhỏ H2S có thể hiện diện.
Xem thêm
sửaGhi chú
sửa- ^ a b c Holleman A. F.; Wiberg E. (2001), Inorganic Chemistry, San Diego: Academic Press, ISBN 0-12-352651-5
- ^ Werner H. (1982). "Novel Coordination Compounds formed from CS2 and Heteroallenes". Coordination Chemistry Reviews. Quyển 43. tr. 165–185. doi:10.1016/S0010-8545(00)82095-0.
Liên kết ngoài
sửa- NPI: Carbon đisunfua Lưu trữ ngày 30 tháng 8 năm 2007 tại Wayback Machine
